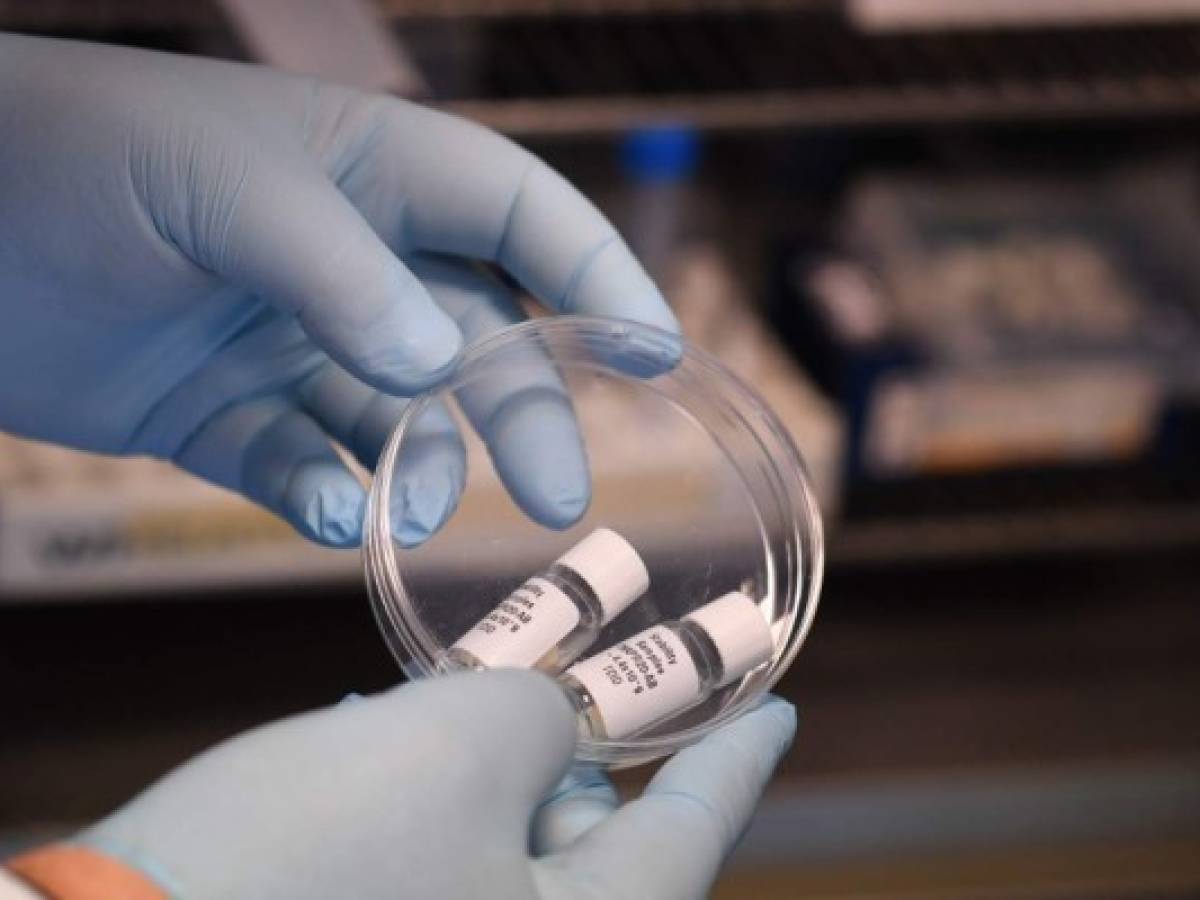
Julio será un mes clave para dos vacunas estadounidenses que tratan de combatir el nuevo coronavirus.
Puede leer: Bill Gates teme que crezca el rechazo a vacunarse por desinformación sobre covid-19
Los grupos estadounidenses Johnson & Johnson y Moderna están listos para seguir con sus últimas fases de prueba.
La primera anunció este miércoles que comenzará ensayos en humanos para una vacuna contra el coronavirus en la segunda mitad de julio, adelantando sus planes iniciales, que preveían hacerlo en septiembre.
En un comunicado, la empresa explicó que ha sido posible 'acelerar el desarrollo clínico' del producto gracias a los buenos datos obtenidos hasta ahora con él y a los contactos con los reguladores.
En este primer ensayo en humanos, la vacuna se probará con 1.045 adultos sanos de entre 18 y 55 años, así como en personas de más de 65 años, y se llevará a cabo en Estados Unidos y Bélgica.
La empresa informó además de que está en discusiones con los reguladores para adelantar también la siguiente fase de las pruebas, para la que por ahora no hay una fecha anunciada. Mientras tanto, la multinacional con sede en New Brunswick (Nueva Jersey, EE.UU.) explicó que está aumentando su capacidad de producción y en discusiones con socios en todo el mundo para asegurar acceso a la vacuna a nivel global.
Si la vacuna es segura y efectiva, Johnson & Johnson tiene el objetivo de suministrar más de mil millones de dosis durante 2021.
Asimismo, la vacuna experimental contra la covid-19 de la biotecnológica estadounidense Moderna, cofinanciada por el gobierno de Estados Unidos, entrará en la tercera y última fase de ensayos clínicos en julio con 30.000 voluntarios, anunció el jueves la compañía.
Se trata de la fase decisiva de los ensayos, que permitirá ver, en una gran muestra de personas sanas, si la vacuna es más efectiva que un placebo para prevenir la infección por el nuevo coronavirus.
Se concluyó el protocolo con la Agencia de Medicamentos de Estados Unidos (FDA) y el ensayo se llevará a cabo en colaboración con los Institutos Nacionales de Salud (NIH).
Moderna está --junto con la Universidad de Oxford, que también lanzó un ensayo a gran escala con 10.000 voluntarios y espera los primeros resultados en septiembre-- a la cabeza en la carrera mundial de vacunas.
La compañía biotecnológica recibió US$483 millones de dólares del gobierno de Estados Unidos.
El 18 de mayo, anunció unos primeros resultados alentadores en un pequeño número de voluntarios (ocho), como parte de la primera fase de los ensayos clínicos.
La fase 2, que incluye 600 voluntarios, comenzó a fines de mayo. La vacunación se realiza en dos dosis separadas de 28 días. La mitad de los participantes recibe un placebo de forma aleatoria.
Si la dosis elegida para las pruebas (100 microgramos) demuestra ser efectiva, Moderna planea producir 500 millones de dosis por año y 'posiblemente hasta 1.000 millones'.
La compañía es una de las cinco en las que la administración del presidente Donald Trump ha apostado en el contexto de su operación 'Warp Speed' (a la velocidad de la luz), según el New York Times, junto con AstraZeneca (socio industrial de vacuna de Oxford), Johnson & Johnson, Merck y Pfizer.
La tecnología de Moderna, basada en el ARN mensajero, nunca ha demostrado ser efectiva contra otros virus. Su objetivo es proporcionar al cuerpo la información genética necesaria para propiciar preventivamente la protección contra el coronavirus.
Actualmente, están en desarrollo al menos 124 vacunas para la COVID-19, según datos de la Organización Mundial de la Salud (OMS), y al menos una decena de ellas están ya en fase de ensayos clínicos.
CON INFORMACIóN DE AGENCIAS EFE / AFP